শুরু করার পূর্বে কিছু কথা।
আমাদের সাইটে বিসিএস সহ সব পরীক্ষার জন্য প্রতিটা বিষয়ে উদাহরণ সহ সমস্ত কিছু সহজ ভাবে ব্যাখ্যা দেওয়া হয় এবং সাথে সব পরিক্ষার এমসিকিউ এর সমাধান সহ দেওয়া হয়। যদি আপনার প্রতিটা বিষয় সম্পর্কে পড়ে ভালো লাগে তাহলে প্লিজ টপিক গুলো শেয়ার করবেন। ধন্যবাদ
ধাতুর ক্ষয়ঃ- কোনাে ধাতু পরিবেশ থেকে পানি ও অক্সিজেন সহযোগে বিক্রিয়া করে ক্ষয়প্রাপ্ত হলে তাকে ধাতু ক্ষয় বলে।
কীভাবে ধাতুর ক্ষয় নিবারণ করা যায়?
বিভিন্ন প্রক্রিয়ায় ধাতুর ক্ষয় নিবারণ করা যায়। যেমন–
- কোনো ধাতুকে ক্ষয় থেকে রক্ষা করতে হলে অবশ্যই খেয়াল রাখতে হবে, ধাতুটি কোনোভাবেই যেন অ্যানোড হিসেবে কাজ করতে না পারে।
- বাইরের কোনো উৎস থেকে তড়িৎ প্রবাহিত করে উভয় তড়িদদ্বারের বিভবের মান সমান অথবা অ্যানোডের জারণ বিভবের মান কমিয়ে ধাতুকে ক্ষয়মুক্ত রাখা যায়।
- ধাতুর পরিবর্তে ধাতু সংকর ব্যবহার করে অ্যানোডের জারণ কমানো যায়।
ধাতুর ক্ষয় রোধ করার কয়েকটি উপায় হলো-
১। গ্যালভানাইজিং
২। পেইটিং ও
৩। ইলেকট্রোপ্লেটিং
আরও জানুন : পদার্থের শ্রেণীবিভাগ, পরিবর্তন ও গঠনসহ এমসিকিউ
বিস্তারিত হলোঃ
১। গ্যালভানাইজিংঃ আমাদের দৈনন্দিন জীবনের বিভিন্ন কাজে আমরা জিংক বা দস্তা ব্যবহার করে থাকি। এর মধ্যে অন্যতম হলো গ্যালভানাইজিং। লোহার তৈরি দ্রব্যসামগ্রীর উপর দস্তার পাতলা আবরণ দেওয়াকে গ্যালভানাইজেশন বলা হয়। জিঙ্ক এর আবরণ লোহাকে বাতাসে অক্সিজেন ও পানি থেকে রক্ষা করে। ফলে মরিচা পড়তে পারে না এবং লোহারও ক্ষয় হয় না।
দস্তার পরিবর্তে টিন দিয়েও অনেক সময় আবরণ দিয়ে ধাতব পদার্থকে ক্ষয় হতে রক্ষা করা যায়।
২। পেইটিংঃ পেইন্টিং বা রঙ করেও ধাতব পদার্থসমূহের ক্ষয় রোধ করা যায়।বাসার রেফ্রিজারেটরে, আলমারি, গাড়ি, স্টিলের আসবাবপত্র এ সবই রং করা হয় পেইন্ট দিয়ে- এদের ক্ষয় রোধ করার জন্য। এই পেইন্ট সময়ের সাথে সাথে নষ্ট হয়ে যেতে পারে। সেক্ষেত্রে যত দ্রুত সম্ভব আবার পেইন্টিং করে নেওয়া ভালো।
৩। ইলেকট্রোপ্লেটিংঃ ইলেকট্রোপ্লেটিং হলো তড়িৎ বিশ্লেষণের মাধ্যমে একটি ধাতুর উপর আরেকটি ধাতুর পাতলা আবরণ তৈরির প্রক্রিয়া। এই প্রক্রিয়ায় সাধারণত নিকেল ক্রোমিয়াম, টিন, সিলভার ও সোনা দিয়ে আবরণ তৈরি করা হয়। এতে একদিকে যেমন ধাতুর ক্ষয় রোধ করা যায়, অন্যদিকে তেমনি আকর্ষণীয় ও চকচকে হয়।
খাবারের কৌটা সাইকেল এগুলোর ক্ষেত্রে লোহার উপর টিনের ইলেকট্রোপ্লেটিং করা হয়।
আরও পড়ুন : পরমাণুর গঠন সম্পর্কে এমসিকিউ সহ বিস্তারিত ।। 1secondschool
ধাতুর ক্ষয়
● কোন ধাতুর পরিবেশ থেকে পানি ও অক্সিজেন সহযোগে বিক্রিয়া করে ক্ষয়প্রাপ্ত হলে তাকে বলে – করোসান বা ধাতুর ক্ষয়।
● মরিচার সংকেত – Fe₂O₃.2H₂O
● ধাতুরর ক্ষয় একটি – তড়িৎ রাসায়নিক প্রক্রিয়া।
● লোহার উপর জিংক ধাতুর প্রলেপ দেয়াকে বলে – গ্যালভানাইজিং।
● ধাতুকে ক্ষয়রোধ করার জন্য তার উপর তড়িৎ প্রলেপন করার পূর্বে ধাতুকে পরিস্কার করা হয় – নাইট্রিক এসিড দিয়ে।
● বনভূমি ধ্বংস হওয়ার একটি কারণ হলো – এসিড বৃষ্টি।
● দালান কোঠার ক্ষয় হয় – এসিড বৃষ্টির সাথে ক্ষারীয় যৌগের ক্রিয়ায়।
● ধাতু নির্মিত সেতু, জাহাজ ও যানবাহন ক্ষয় হয় – এসিড বৃষ্টির ফলে।
● ওজোন স্তরের ক্ষয়ের জন্য দায়ী – জেট বিমান থেকে নির্গত নাইট্রোজেন অক্সাইড।
● নাইট্রোজেন অক্সাইড ওজোনকে নিয়োজিত করে পরিণত করে – অক্সিজেন গ্যাসে।
● দীর্ঘদিন থাকলেও ক্ষয় বা নষ্ট হয় না – পলিথিন।
● ওজোন স্তর ক্ষয়ের জন্য দায়ী মূলত – ক্লোরোফ্লোরো কার্বন গ্যাস।
● CFC অাবিষ্কার করেন – T Midgby
● পরিবেশবাদী ফ্রিজ হলো – CFC বিহীন ফ্রিজ।
● CFC এর দূষণরোধ করার জন্য বর্তমানে CFC এর পরিবর্তে ব্যবহার করা হয় – গ্যাজেলিয়াম।
● যে গ্যাস মানবদেহের জন্য উপকারী ও অপকারী – ওজোন।
● এসিড বৃষ্টি হয় বাতাসে – সালফার ডাই অক্সাইডের অাধিক্যের কারণে।
● খরপানির ম্যাগনেসিয়াম ক্লোরাইড এর পানি বিশ্লেষণের ফলে হাইড্রোক্লোরিক এসিড উৎপন্ন হয় – যা লোহার সাথে বিক্রিয়া করে বয়লারের ক্ষয় করে।
● বৃষ্টি চলাকালীন বজ্রপাতের সময় বায়ুর অক্সিজেন ও নাইট্রোজেন বিদ্যুৎস্ফুলিঙ্গের উপস্থিতিতে পরস্পর যুক্ত হয়ে উৎপন্ন করে – নাইট্রিক অক্সাইড।
● মানুষ ও জীবজন্তুর ত্বকে লাগলে ক্ষতের সৃষ্টি করে – নাইট্রিক এসিড।
● তেজস্ক্রিয় পদার্থের পরমাণুর মধ্যস্থ নিউক্লিয়াস – অস্থায়ী হয়।
আরও পড়ি : কার্বন । কার্বনের রুপভেদ – বৈশিষ্ট – ধর্ম ।
● তেজস্ক্রিয় পরমাণুর ভাঙ্গন বা ক্ষয় চলতে থাকে – যতক্ষণ না এটি একটি অতেজস্ক্রিয় কণা বিকিরণের মাধ্যমে।
● তেজস্ক্রিয় ক্ষয়ে রূপান্তরিত পরমাণুকে বলা হয় – জাতক পরমাণু।
● একটি তেজস্ক্রিয় পদার্থের পরমাণু ভাঙন বা ক্ষয়ের মাধ্যমে অন্য একটি অতেজস্ক্রিয় পরামাণুতে পরিণত হওয়াকে বলে – তেজক্রিয় ক্ষয়।
● তেজস্ক্রিয় ক্ষেত্রের সূত্র অাবিষ্কার করেন – রাদারফোর্ড ও সডি।
● তেজস্ক্রিয় ক্ষয় মেনে চলে – সূচকীয় সূত্র।
● তেজস্ক্রিয় ক্ষয় একটি – স্বতঃস্ফুর্ত ঘটনা।
● তেজস্ক্রীয় ক্ষয়ের মাধ্যমে নির্গত তেজস্ক্রিয় রশ্মি – প্রাণীর জন্য ক্ষতিকর।
● তেজস্ক্রিয় রশ্মির ক্ষতিকর প্রভাব – বংশপরম্পরা চলতে থাকে।
*) সবচেয়ে দ্রুত ক্ষয় প্রাপ্ত হয় যে ধাতু ➟দস্তা( জিংক)
*) সবচেয়ে হালকা ধাতু ➟ লিথিয়াম
*) সবচেয়ে সক্রিয় ধাতু ➟ পটাসিয়াম
*) সবচেয়ে মূল্যবান ধাতু ➟ প্লাটিনাম
*) সবচেয়ে শক্ত পদার্থ ➟ হীরক
*). সবচেয়ে ভারী তরল পদার্থ ➟ পারদ ও সিজিয়াম
*). স্বাভাবিক তাপমাত্রায় তরল ধাতু ➟ পারদ
*). গলনাংক সবচেয়ে কম যে ধাতুর ➟ পারদ
তেজস্ক্রিয় ক্ষয় কী?
তেজস্ক্রিয় ক্ষয় প্রক্রিয়া হ’ল অস্থির আইসোটোপগুলি নির্গত বিকিরণের মাধ্যমে ক্ষয় হয়। অস্থির আইসোটোপগুলি অস্থিতিশীল নিউক্লিয়াসহ পরমাণু oms নিউক্লিয়ায় প্রচুর পরিমাণে প্রোটনের উপস্থিতি বা নিউক্লিয়ায় একটি উচ্চ সংখ্যক নিউট্রনের উপস্থিতির মতো বিভিন্ন কারণে একটি পরমাণু অস্থির হয়ে উঠতে পারে। এই নিউক্লিয়াগুলি স্থিতিশীল হওয়ার জন্য তেজস্ক্রিয় ক্ষয় হয়।
যদি অনেক বেশি প্রোটন থাকে এবং অনেক বেশি নিউট্রন থাকে তবে পরমাণুগুলি ভারী হয়। এই ভারী পরমাণুগুলি অস্থির। সুতরাং, এই পরমাণুগুলি তেজস্ক্রিয় ক্ষয় হতে পারে। অন্যান্য পরমাণুগুলিও তাদের নিউট্রন: প্রোটন অনুপাত অনুযায়ী তেজস্ক্রিয় ক্ষয় হতে পারে। যদি এই অনুপাতটি খুব বেশি হয় তবে এটি নিউট্রন সমৃদ্ধ এবং অস্থির। যদি অনুপাতটি খুব কম হয় তবে এটি প্রোটন সমৃদ্ধ পরমাণু এবং অস্থির। পদার্থগুলির তেজস্ক্রিয় ক্ষয় তিনটি প্রধান উপায়ে হতে পারে।
- আলফা নিঃসরণ / ক্ষয়
- বিটা নিঃসরণ / ক্ষয়
- গামা নির্গমন / ক্ষয়
আলফা নিঃসরণ
একটি আলফা কণা হিলিয়াম পরমাণুর অনুরূপ। এটি 2 প্রোটন এবং 2 নিউট্রন নিয়ে গঠিত। আলফা কণা একটি +2 বৈদ্যুতিক চার্জ বহন করে কারণ 2 প্রোটনের ধনাত্মক চার্জকে নিরপেক্ষ করার জন্য কোনও ইলেকট্রন নেই। আলফা ক্ষয়ের কারণে আইসোটোপগুলি 2 টি প্রোটন এবং 2 নিউট্রন হারাতে পারে। সুতরাং, একটি তেজস্ক্রিয় আইসোটোপের পারমাণবিক সংখ্যা 2 ইউনিট এবং 4 ইউনিট থেকে পারমাণবিক ভর হ্রাস পেয়েছে। ইউরেনিয়ামের মতো ভারী উপাদানগুলি আলফা নির্গমন করতে পারে।
বিটা নির্গমন
বিটা নিঃসরণের প্রক্রিয়াতে (β), একটি বিটা কণা নির্গত হয়। বিটা কণার বৈদ্যুতিক চার্জ অনুযায়ী, এটি হয় ধনাত্মক চার্জযুক্ত বিটা কণা বা negativeণাত্মক চার্জযুক্ত বিটা কণা হতে পারে। যদি এটি β – নির্গমন হয় তবে নির্গত কণা একটি বৈদ্যুতিন। যদি এটি β + নিঃসরণ হয় তবে কণাটি একটি পজিট্রন। পজিট্রন হ’ল একটি কণা যা তার ইলেক্ট্রনের চার্জ বাদে একই বৈশিষ্ট্যযুক্ত having পজিট্রনের চার্জটি ইতিবাচক এবং বৈদ্যুতিনের চার্জ নেতিবাচক। বিটা নিঃসরণে একটি নিউট্রন প্রোটন এবং একটি ইলেক্ট্রন (বা পজিট্রন) এ রূপান্তরিত হয়। সুতরাং, পারমাণবিক ভর পরিবর্তন করা হবে না, কিন্তু পারমাণবিক সংখ্যা এক ইউনিট দ্বারা বৃদ্ধি করা হয়।
গামা নির্গমন
গামা বিকিরণ কণা হয় না। সুতরাং, গামা নির্গমন পারমাণবিক সংখ্যা বা একটি পরমাণুর পারমাণবিক ভর পরিবর্তন করে না। গামা বিকিরণটি ফোটন দিয়ে তৈরি। এই ফোটনগুলি কেবলমাত্র শক্তি বহন করে। সুতরাং, গামা নিঃসরণের ফলে আইসোটোপগুলি তাদের শক্তি প্রকাশ করে।
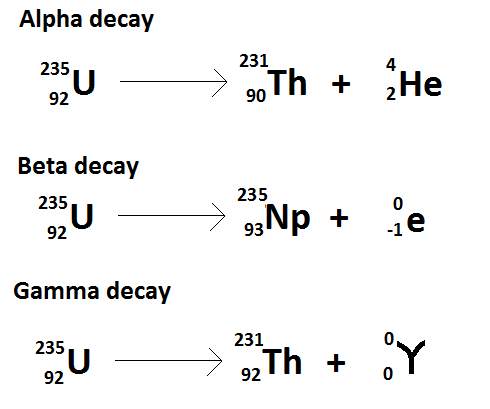
চিত্র 1: ইউরেনিয়াম -235 এর তেজস্ক্রিয় ক্ষয়
ইউরেনিয়াম -235 একটি তেজস্ক্রিয় উপাদান যা প্রাকৃতিকভাবে পাওয়া যায়। এটি বিভিন্ন পরিস্থিতিতে তিন ধরণের তেজস্ক্রিয় ক্ষয়ে যেতে পারে।
হাফ লাইফ কি
তেজস্ক্রিয় ক্ষয়ের মধ্য দিয়ে তার প্রাথমিক ভর বা ঘনত্বের অর্ধেক হয়ে যাওয়ার জন্য কোনও পদার্থের অর্ধেক জীবন সেই পদার্থের দ্বারা নেওয়া সময়। এই শব্দটি টি 1/2 প্রতীক দেওয়া হয়। অর্ধজীবন শব্দটি ব্যবহার করা হয়েছে কারণ কোনও ব্যক্তির পরমাণু কখন ক্ষয় হতে পারে তা অনুমান করা যায় না। তবে, তেজস্ক্রিয় উপাদানের অর্ধ নিউক্লিয়াসে নেওয়া সময়টি পরিমাপ করা সম্ভব।
অর্ধেক জীবন নিউক্লিয়াসির সংখ্যা বা ঘনত্ব সম্পর্কিত কোনওটি হতে পারে। বিভিন্ন আইসোটোপ বিভিন্ন অর্ধ জীবন আছে। সুতরাং, অর্ধেক জীবন পরিমাপ করে আমরা একটি নির্দিষ্ট আইসোটোপের উপস্থিতি বা অনুপস্থিতির পূর্বাভাস দিতে পারি। অর্ধ জীবন পদার্থ, তাপমাত্রা, চাপ বা অন্য কোনও প্রভাবের শারীরিক অবস্থার থেকে পৃথক।
অর্ধ জীবনের সূত্র:
কোথায়,
- N0 প্রাথমিক পরিমাণ।
- N(t) এর পরে উপস্থিত পরিমাণ t সেকেন্ড
- t1-2 অর্ধেক জীবন।
- lifetime গড় জীবনকাল (+ Ve),
- ay ক্ষয় ধ্রুবক (+ Ve)।
তিনটি পরামিতি t 1 ⁄ 2, τ, এবং λ সমস্ত নিম্নলিখিত উপায়ে সরাসরি সম্পর্কিত
আরও দেখুন : এসিড, ক্ষার, লবণ (Acids, Bases and Salts)
তেজস্ক্রিয় ক্ষয় এবং অর্ধ জীবনের মধ্যে সম্পর্ক
তেজস্ক্রিয় ক্ষয় এবং তেজস্ক্রিয় পদার্থের অর্ধেক জীবনের মধ্যে সরাসরি সম্পর্ক রয়েছে। তেজস্ক্রিয় ক্ষয়ের হার অর্ধেক জীবনের সমতলে পরিমাপ করা হয়। উপরের সমীকরণ থেকে, আমরা তেজস্ক্রিয় ক্ষয়ের হার গণনার জন্য আরেকটি গুরুত্বপূর্ণ সমীকরণ অর্জন করতে পারি।
Solutionঃ
আমাদের পোষ্ট গুলো প্রতিনিয়ত আপডেট করা হয়। বিসিএস,প্রাইমারি সহ সব পরীক্ষার প্রতিনিয়ত প্রশ্ন অনুযায়ী পোষ্ট গুলো আমরা আপডেট করি। সবার জন্য শুভ কামনা রইলো।